Seit Jahrzehnten werden Aminosäuren zu medizinischen Formeln hinzugefügt, beispielsweise als Stabilisatoren in Insulin. Diese kleinen Moleküle verhindern, dass Proteine (d. h. grössere Teilchen) in unerwünschter Weise miteinander interagieren. Seit Jahrzehnten wissen die Wissenschaftler, dass dies funktioniert - aber sie wissen nicht, warum.
Ein internationales Team unter der Leitung des Labors für Nanomaterialien und supramolekulare Grenzflächen der Fakultät für Ingenieurwissenschaften und Technik der EPFL erklärt dieses Phänomen nun endlich und zeigt eine grundlegende stabilisierende Wirkung aller kleinen Moleküle in Lösung. Diese Entdeckung, die in Zusammenarbeit mit dem MIT (Alfredo Alexander-Katz) und der Southern University of Science and Technology in China (EPFL-Alumnus Zhi Luo) gemacht wurde, wurde in Nature veröffentlicht .
"Wenn Proteine in einer Lösung suspendiert sind, ändern sie ständig ihre Form um eine zentrale Konfiguration herum. Die vorherrschende Theorie ist daher, dass Aminosäuren die Fehlfaltung von Proteinen verhindern", erklärt Ting Mao, die kürzlich an der EPFL promoviert hat und Hauptautorin ist.
"Unsere Studie zeigt, dass dies nicht der Fall ist. Tatsächlich hat die stabilisierende Wirkung von Aminosäuren wenig mit Biologie zu tun, sondern ist vielmehr eine allgemeine Eigenschaft aller kleinen Moleküle im Vergleich zu grösseren Partikeln, sogenannten Kolloiden, in einer Lösung."
Anziehung und Abstossung ins Gleichgewicht bringen
Um diesen kolloidalen Effekt kleiner Moleküle zu verstehen, nimmt Francesco Stellacci, Leiter des Labors für Nanomaterialien und supramolekulare Schnittstellen, das Bild von zwei Kollegen, die in einem Flur aufeinander zugehen."Nehmen wir an, diese beiden Kollegen verstehen sich sehr gut und wollen immer stehen bleiben, um sich zu unterhalten. Wenn der Flur leer ist, werden sie sich sofort entdecken und aufeinander zugehen. Ist der Gang jedoch überfüllt, kann es sein, dass sie sich erst sehen, wenn sie aneinander vorbeigehen, oder sich sogar ganz verfehlen", erläutert Francesco Stellacci. "Dieses Phänomen, das als filternde Anziehung bezeichnet wird, ist die Art und Weise, wie Aminosäuren auf grössere Partikel wirken: Sie übernehmen die Rolle der Menschenmenge im Flur, entmutigen die Interaktion im Vorbeigehen und verhindern spontane Flurgespräche."
Unser Endziel ist es, vorherzusagen, welche Moleküle welche Proteine in welcher Menge stabilisieren können - was in der biomedizinischen Forschung derzeit noch durch Versuch und Irrtum geschieht.
Francesco Stellacci
Seit mehr als einem Jahrhundert kennen Wissenschaftler die umgekehrte Wirkung von Salzen: Sie filtern Abstossung heraus. Im Flurbeispiel spielt das Salz auch die Rolle der Menschenmenge, doch in diesem Fall hindert es zwei unfreundliche Kollegen daran, eine lästige Interaktion zu vermeiden.
"Wir haben herausgefunden, dass Aminosäuren in Wirklichkeit Anti-Salz sind, da sie eine umgekehrte Filterwirkung haben. Das kann man sogar in der Natur sehen: Wenn eine Pflanze mit Salzwasser gegossen wird, produzieren ihre Zellen nachweislich mehr Aminosäuren, um sie zu stabilisieren, wenn sie durch die erhöhte Salzkonzentration gestresst sind", sagt Quy Ong, Forscher und Koautor an der EPFL
Bessere Kontrolle der molekularen Interaktionen
Diese Arbeit spricht dafür, in künftigen wissenschaftlichen Studien die Aminosäurekonzentrationen anzugeben, meinen die Forscherinnen und Forscher. "In der Biologie würde man nie ein Experiment durchführen, ohne die Ionenkonzentration (Salz) einer Lösung anzugeben. Unsere Arbeit zeigt, dass die Konzentrationen von Aminosäuren genauso viel Einfluss haben und daher genauso genau berichtet werden müssen", sagt Francesco Stellacci.Tatsächlich nutzt der Professor das ungenutzte Potenzial dieser molekularen Effekte bereits im Rahmen des ERC Advanced Grant, den er gerade erhalten hat. "Wir wollen verstehen, wie kleine Moleküle wie Aminosäuren für eine gesunde biologische Funktion entscheidend sind. Mit der Unterstützung unseres ERC-Fonds ist es unser ultimatives Ziel, vorherzusagen, welche Moleküle welche Proteine in welcher Menge stabilisieren können - was in der biomedizinischen Forschung derzeit durch Versuch und Irrtum geschieht."
Referenzen
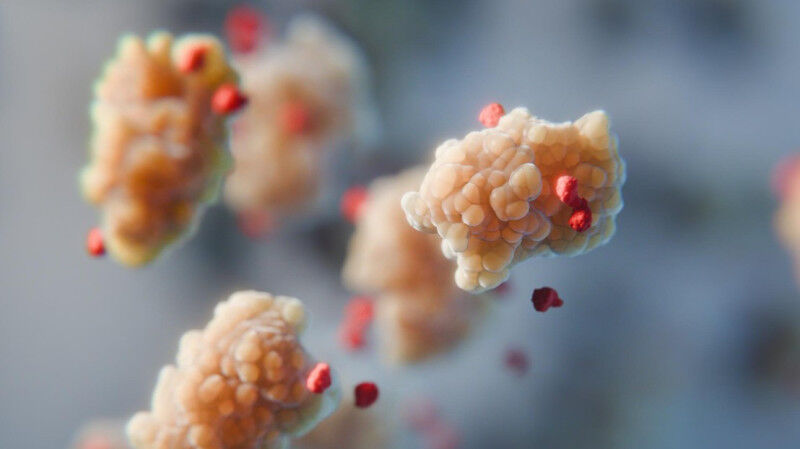
Mao, T., Xu, X., Winkler, P.M. et al. Stabilizing effect of amino acids on protein and colloidal dispersions. Nature (2025). https://doi.org/10.1038/s41586-025-09506-wAminosäuren (rot) "filtern" die Anziehungskraft von Proteinen (gelb). 2025 SuNMIL CC BY SA