Une étude internationale dirigée par l’Université de Bâle montre que les complexes de pores nucléaires - de minuscules passages dans la membrane du noyau cellulaire - ne sont pas rigides ou gélatineux, comme on le pensait jusqu’à présent. Leur intérieur est organisé de manière dynamique, bouge et se modifie constamment. Ces résultats modifient notre compréhension d’un processus de transport important dans les cellules et ont des répercussions sur les maladies et les thérapies possibles.
Le noyau cellulaire ressemble à un coffre-fort bancaire que les complexes de pores nucléaires (NPC) protègent comme un système de sécurité très sophistiqué. Seules les protéines possédant la bonne ’clé’ - des facteurs de transport spéciaux - bénéficient d’un accès exclusif. De cette manière, le système contrôle quelles substances entrent dans le noyau cellulaire ou le quittent. Ce contrôle étroit est indispensable pour garantir une communication fluide entre le génome protégé à l’intérieur et les machines cellulaires à l’extérieur.
De nouvelles connaissances biologiques grâce aux nanosciences
Malgré leur importance, les processus internes des complexes de pores nucléaires restent une énigme. Leur canal de transport est tapissé de filaments protéiques très flexibles - les nucléoporines FG (FG Nups). Elles forment une barrière sélective dont la structure ultrafine reste cachée même aux microscopes électroniques les plus performants. Comme les FG Nups peuvent former des structures de type gel à l’extérieur des cellules, des modèles plus anciens ont comparé la fonction des complexes de pores nucléaires à celle d’un tamis rigide.
Aujourd’hui, une équipe dirigée par Roderick Lim, professeur Argovia de nanobiologie au Biozentrum et au Swiss Nanoscience Institute de l’Université de Bâle, a utilisé la microscopie à force atomique à haute vitesse (HS-AFM) pour filmer des mouvements inédits à l’échelle nanométrique avec une résolution de l’ordre de la milliseconde directement à l’intérieur des pores. Les chercheurs ont maintenant publié la découverte des restructurations extraordinaires au sein des complexes de pores nucléaires dans la revue spécialisée ’Nature Cell Biology’.
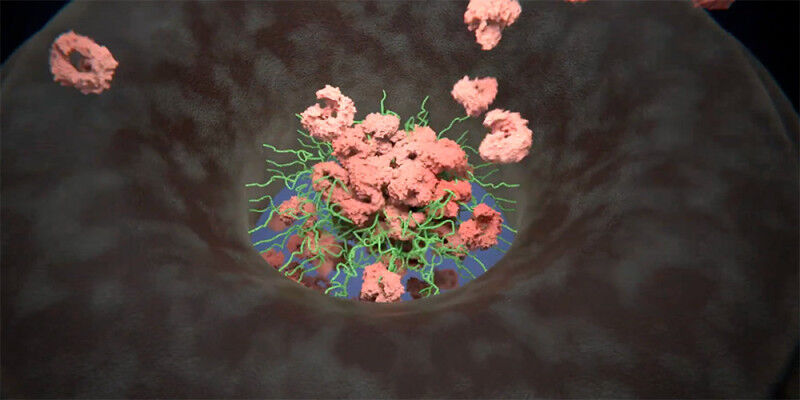
Des filaments de protéines hautement dynamiques, appelés FG-Nups (en vert), sont ancrés à l’intérieur du pore. Dans des conditions vivantes, les facteurs de transport (rose) qui transportent le fret interagissent avec les FG-nups et forment en vrac un bouchon central qui contribue à l’organisation d’une barrière de transport dynamique. Le transport sélectif peut se faire de préférence à travers la région environnante. Pour des raisons de clarté, les molécules de fret ne sont pas représentées et la densité des FG-Nup a été réduite. (Animation : Enrique Sahagun, Scixel)
’La barrière du complexe de pores nucléaires est organisée de manière lâche par un bouchon central mobile, dont les composants sont longtemps restés mystérieux. Il s’est avéré qu’il est constitué d’un mélange dynamique de facteurs de transport, de molécules de fret et de FG-Nups qui se mélangent le long de l’axe central du pore. Il en résulte un système hautement adaptable qui renforce la barrière tout en assurant un transport sélectif rapide’, explique Lim.
Nager avec le courant
L’équipe a découvert cette organisation dynamique en étudiant les complexes de pores nucléaires de cellules de levure. Les films AFM à grande vitesse qui en ont résulté ont également montré les mouvements fluides des noyaux FG qui ’rayonnent’ vers le bouchon central à l’intérieur du pore.
lorsque nous avons observé des complexes de pores nucléaires isolés pendant une période prolongée dans des conditions contrôlées, le bouchon central des complexes de pores nucléaires a disparu. Si nous ajoutions à nouveau des facteurs de transport nucléaires, il se formait à nouveau", rapporte le Dr Toshiya Kozai, premier auteur de l’étude. Fait remarquable, les facteurs de transport ont également rétabli une fonction de barrière similaire aux complexes de pores nucléaires dans les nanopores artificiels, ce qui indique la généralité de ce mécanisme.
Les hydrogels ressemblent à des éponges trouées
Les complexes de pores nucléaires sont souvent comparés aux hydrogels. cela s’explique par le fait que les FG-Nups forment des hydrogels in vitro - c’est-à-dire en tube à essai - qui sont toutefois mille fois plus grands que les complexes de pores nucléaires. Mais ils sont constitués de structures fibreuses enchevêtrées qui sont tout simplement trop grandes pour s’adapter à un complexe de pores centraux, et encore moins à l’ensemble du corps de l’hydrogel lui-même’, explique Lim.
lorsque nous avons examiné les hydrogels de plus près, nous avons constaté qu’ils étaient parsemés de trous de forme et de taille irrégulières, comme une éponge de cuisine. Beaucoup de ces trous étaient aussi grands que des complexes de pores nucléaires, voire plus grands. Ils pouvaient éventuellement imiter un comportement similaire à celui des complexes de pores nucléaires’.
Défis pour l’avenir
Le comportement dynamique auto-organisé mis en évidence par l’étude offre une vision unifiée des complexes de pores nucléaires, conforme aux observations structurelles et biochimiques de longue date - avec des implications allant de la biologie cellulaire fondamentale à la conception de filtres intelligents et de systèmes de délivrance de médicaments.
La restriction de l’état dynamique des pores affecte le transport sélectif vers le noyau cellulaire, ce qui illustre l’importance de ce comportement pour le bon fonctionnement de la cellule.
le prochain défi consiste à comprendre comment les cellules ajustent finement ces remarquables nanomachines en réponse à des besoins changeants - comment les pores s’adaptent au stress, régulent la croissance et, lorsqu’ils sont obstrués, contribuent aux maladies", ajoute Michael Rout de l’Université Rockefeller, qui a codirigé le travail.
Ce travail est le fruit d’une collaboration internationale entre des chercheurs du Biocentre et du Swiss Nanoscience Institute de l’Université de Bâle (Suisse), de la Rockefeller University (New York, États-Unis), de la Ikerbasque Foundation for Science (Bilbao, Espagne), le Biofisika Institute-CSIC-UPV/EHU-Fundacion Biofisika Bizkaia (Leioa, Espagne), l’Université de Groningen (Pays-Bas), l’Université hébraïque de Jérusalem (Israël), l’Université de Californie, San Francisco (États-Unis), l’Université de Yale (West Haven, États-Unis), et la Yale School of Medicine (New Haven, CT, États-Unis).
Publication originale
Kozai, T., Fernandez-Martinez, J., Kapinos, L.E. et al.
Les caryophérines remodèlent l’organisation dynamique de la barrière de transport du complexe de pore nucléaire.
Nature Cell Biology (2025), doi : 10.1038/s41556-025-01812-9