Des chercheurs de l’Université de Bâle ont modifié une enzyme naturelle de manière à ce qu’elle catalyse une réaction chimique extrêmement exigeante. Des molécules complexes pour des médicaments et des produits chimiques fins pourraient ainsi être produites de manière plus écologique et plus efficace.
Les catalyseurs font partie des outils les plus importants sur la voie d’une chimie verte plus durable. Ils accélèrent les réactions chimiques, les rendent plus efficaces et plus faciles à contrôler. Ils permettent ainsi d’économiser de l’énergie, des déchets et des coûts lors de la fabrication de produits très divers. La recherche de nouveaux catalyseurs occupe la chimie depuis le 20e siècle.
Une méthode prometteuse avec un hic
Récemment, le transfert d’atomes d’hydrogène par hydrure métallique (MHAT) a été considéré comme une méthode catalytique prometteuse. La réaction MHAT permet de construire efficacement des molécules complexes avec des fonctions spécifiques. Une combinaison d’un métal et d’un atome d’hydrogène - ce qu’on appelle un hydrure métallique - transfère un atome d’hydrogène à un hydrocarbure avec au moins une double liaison. Il en résulte un site particulièrement réactif qui forme ensuite une liaison avec un groupe d’atomes. Ce groupe fonctionnel détermine les propriétés chimiques de la molécule.
La réaction MHAT peut transformer un substrat plat et bidimensionnel en une molécule complexe avec une architecture tridimensionnelle. Il est toutefois difficile de contrôler l’agencement tridimensionnel précis des atomes dans la molécule. En effet, bien que deux molécules soient composées des mêmes atomes, elles peuvent se comporter comme une image et un reflet et ne pas être amenées à coïncider. On peut se représenter les deux variantes de molécules - appelées énantiomères - comme des mains gauche et droite.
Pour l’industrie pharmaceutique ou la fabrication de produits chimiques fins, la création d’une certaine configuration est toutefois essentielle. En effet, les deux molécules inversées peuvent avoir des propriétés biologiques différentes. Par exemple, l’image miroir d’un médicament peut avoir un effet complètement différent, voire toxique.
Une enzyme produit la configuration souhaitée
Des chercheurs de l’Université de Bâle ont maintenant réussi à combiner la chimie MHAT avec la catalyse enzymatique pour produire de manière ciblée un énantiomère souhaité. Pour cette étude publiée dans la revue spécialisée ’Nature’, l’équipe de Thomas R. Ward a utilisé le principe clé-serrure des enzymes naturelles.
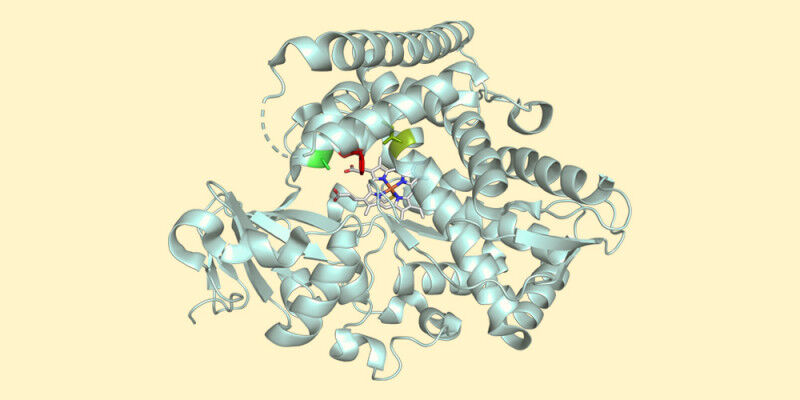
Chaque enzyme possède un centre actif - une sorte de poche dans laquelle seule une ou quelques molécules spécifiques s’insèrent comme la clé dans la serrure. Le groupe de recherche a transformé une hémoprotéine - une enzyme très répandue dans la nature - de manière à ce que la réaction MHAT se produise dans le centre actif de l’enzyme. Grâce à l’environnement spécifique de cette poche enzymatique, l’énantiomère souhaité est produit dans 98 cas sur 100, car son image miroir ne s’intégrerait pas dans le centre actif.
Cette réaction est extrêmement difficile à réaliser avec les outils chimiques habituels. Grâce à l’enzyme, elle se déroule non seulement avec précision, mais aussi avec efficacité. Les enzymes ont développé leurs propriétés catalytiques au cours de millions d’années afin de maintenir la vie avec une dépense énergétique minimale. Elles sont en outre intéressantes pour la chimie en raison de leur respect de l’environnement. jusqu’à présent, aucune enzyme capable de réaliser la réaction MHAT n’était connue", explique le Dr Xiang Zhang, premier auteur.
Cette percée dans le domaine de la catalyse enzymatique ouvre la voie à une production plus écologique et plus efficace d’une multitude de structures chimiques complexes - par exemple pour l’industrie pharmaceutique ou pour la fabrication de produits naturels. Cette recherche pionnière s’inscrit dans le cadre du pôle de recherche national ’Molecular Systems Engineering’, dirigé par Thomas Ward.
La spécificité de l’enzyme est cependant à la fois une malédiction et une bénédiction : en effet, si les chercheurs souhaitent utiliser l’enzyme sur une autre substance de départ, ils doivent d’abord adapter à nouveau la structure de l’enzyme. Le groupe de recherche se consacre désormais à ce défi et cherche en outre un moyen plus durable de produire l’hydrure métallique nécessaire à la réaction.
Publication originale
Xiang Zhang, Dongping Chen, María Élvarez, Thomas R. Ward
Repurposing haemoproteins for asymmetric metal-catalysed H atom transfer
Nature (2025), doi : 10.1038/s41586-025-09308-0




