Eines der grössten Hindernisse bei der Entwicklung von Arzneimitteln ist die Löslichkeit. Viele vielversprechende Arzneimittelmoleküle lösen sich im Körper nicht gut genug auf, was ihre Aufnahme, insbesondere in Tablettenform, erschwert. Um dieses Hindernis zu überwinden, wenden sich die Wissenschaftler häufig "amorphen" Formen von Arzneimitteln zu. Im Gegensatz zu kristallinen Festkörpern, bei denen sich die Atome in einem geordneten Gitter aneinanderreihen, handelt es sich bei amorphen Materialien um ein molekulares Durcheinander. Diese Unordnung kann die Löslichkeit erheblich erhöhen, hat aber einen hohen Preis: Instabilität. Mit der Zeit können sich amorphe Medikamente in Kristallen neu anordnen und so ihre Wirksamkeit verlieren.
Um dies zu verhindern, müssen Wissenschaftler verstehen, was die Stabilität amorpher Medikamente aufrechterhält. Doch das ist schwierig. Diese Materialien sind so ungeordnet, dass herkömmliche Techniken wie die Röntgenkristallografie nicht funktionieren. Bis vor kurzem hatte noch niemand die vollständige 3D-Atomstruktur eines amorphen pharmazeutischen Feststoffs kartografiert.
Nun haben Forscherinnen und Forscher unter der Leitung von Lyndon Emsley von der EPFL und Staffan Schantz von AstraZeneca eine neue, effiziente Methode entwickelt, um die Struktur auf atomarer Ebene von amorphen Medikamenten, die bei Diabetes eingesetzt werden, zu kartieren. Die Forscherinnen und Forscher griffen auf eine von ihnen 2023 entwickelte Methode zurück, die NMR-Kristallographie mit maschinellem Lernen und Molekulardynamik-Simulationen kombiniert, um zum ersten Mal eine experimentell validierte 3D-Struktur auf atomarer Ebene eines amorphen pharmazeutischen Feststoffs zu erstellen.
Mithilfe dieser Methode konnte das Team einen der experimentellen GLP-1-Rezeptoragonisten von AstraZeneca untersuchen, eine Art von Medikament zur Behandlung von Typ-2-Diabetes und Fettleibigkeit. Diese Medikamente werden normalerweise injiziert, aber Wege zu finden, stabile und wirksame orale Versionen herzustellen, könnte für Patientinnen und Patienten auf der ganzen Welt einen grossen Unterschied machen.
Das Team hat zunächst mithilfe der Festkörper-Kernspinresonanz (NMR) gemessen, wie die Atomkerne des Medikaments auf Magnetfelder reagieren. Diese Messungen ergaben Verteilungen der chemischen Verschiebungen für 17 Kohlenstoff- und 16 Wasserstoffatome im Molekül.
Die Wissenschaftler simulierten dann mithilfe von Supercomputern über neun Millionen mögliche Molekülumgebungen und wandten ein maschinelles Lernwerkzeug namens ShiftML2 an, um die entsprechenden chemischen Verschiebungen vorherzusagen. Indem sie die Vorhersagen mit den Experimenten abglichen, wählten sie die wahrscheinlichsten Strukturen aus
Wasserstoffbrückenbindungen sind der Schlüssel
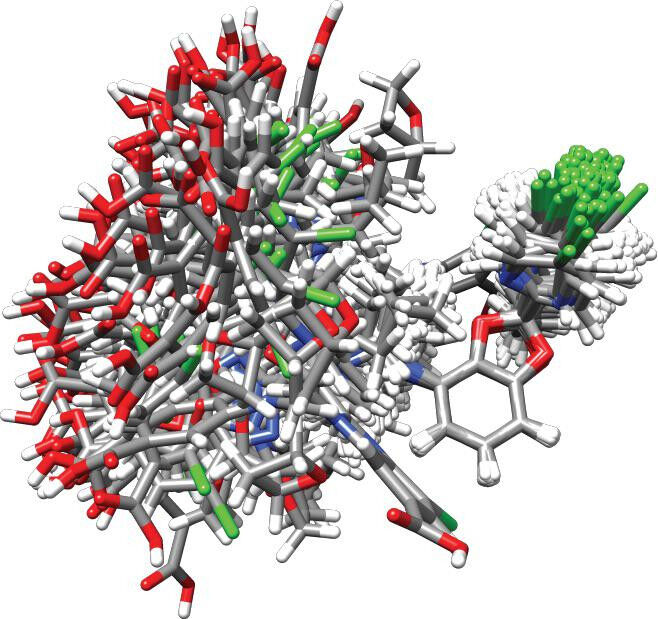
Durch die Kombination von experimentellen Daten mit fortgeschrittenen Simulationen konnte das Team feststellen, welche Konformationen und molekularen Wechselwirkungen innerhalb der amorphen Struktur tatsächlich existierten. Die Wissenschaftler stellten fest, dass die Arzneimittelmoleküle dazu neigen, Wasserstoffbrückenbindungen untereinander oder mit den umgebenden Wassermolekülen zu bilden. Diese Bindungen fungieren als molekulare "Anker" und verringern die Neigung der Moleküle, sich in einer kristallinen und weniger löslichen Struktur neu anzuordnen, insbesondere wenn Wassermoleküle beteiligt sind.Die Analyse zeigte sogar, welche zyklischen Strukturen des Moleküls dazu neigten, bestimmte Orientierungen anzunehmen, die dabei helfen, die Kristallisation zu verhindern. Beispielsweise verdrehten sich bestimmte Teile des Moleküls, wie die Benzodioxol- und Benzimidazolringe, eher in bestimmten Winkeln, insbesondere um -150° und -60° für den Benzodioxolring im Vergleich zum Piperazinring.
Diese "bevorzugten" Verdrehungen helfen, das Molekül in einer stabilen, nicht-kristallinen Form einzuschliessen, was es schwieriger macht, das Material in eine kristalline Struktur umzubauen, ein Prozess, der die Löslichkeit des Medikaments und im weiteren Sinne seine Wirksamkeit im Körper erheblich verringern würde
Eine revolutionäre Methode
Die Studie ergab auch einen bedeutenden methodischen Fortschritt. Anstatt sich allein auf Computervorhersagen zu verlassen, um zu bestimmen, welche Molekülstrukturen stabil sein sollten - ein Ansatz, der manchmal wichtige reale Verhaltensweisen übersehen kann - validierten die Forscherinnen und Forscher ihre Modelle anhand von realen experimentellen Daten aus NMR-Messungen.Das bedeutet, dass sie die genauen Anordnungen auf atomarer Ebene, die in dem amorphen Medikament vorhanden sind, mit hoher Zuverlässigkeit bestätigen konnten. Indem sie ihre Computermodelle gegen tatsächliche experimentelle Beobachtungen filterten, erstellten sie eine neuartige und zuverlässige 3D-Karte eines amorphen pharmazeutischen Feststoffs.
"Dies ist ein beispielloser Grad an struktureller Detailliertheit, und die Erkenntnisse über die Stabilisierungsmechanismen der amorphen Form dieses GLP-1R-Agonisten, die er liefert, sind ein grosser Schritt nach vorn für das Verständnis amorpher Arzneiformen", sagte Lyndon Emsley.
Für GLP-1R-Agonisten, die häufig zur Behandlung von Typ-2-Diabetes und Fettleibigkeit eingesetzt werden, könnte dies letztendlich zu wirksamen oralen Alternativen zu Injektionen führen, die den Komfort für die Patientin oder den Patienten und die Therapietreue deutlich verbessern




