Des scientifiques de l’Université de Lausanne ont mis en évidence un mécanisme inédit par lequel le système immunitaire identifie l’endotoxine, une molécule clé présente dans la membrane de certaines bactéries. Publiée dans la revue scientifique Immunity, cette découverte ouvre des perspectives prometteuses pour la prise en charge des infections sévères et la prévention du choc septique.
Le système immunitaire inné constitue la première barrière de défense de l’organisme. Il repose sur la capacité à reconnaître rapidement des signatures moléculaires propres aux microbes - absentes de nos cellules - afin de déclencher une réponse inflammatoire et antimicrobienne immédiate. Ce mécanisme est essentiel pour contenir l’invasion de pathogènes avant que l’infection ne se propage.
L’endotoxine, déclencheur majeur des formes graves d’infection
Parmi ces signaux microbiens, le lipopolysaccharide (LPS) occupe une place centrale. Ce glycolipide, principal constituant de la membrane externe des bactéries dites Gram négatives, est connu depuis plus d’un siècle pour sa capacité à provoquer des réactions inflammatoires intenses. Longtemps identifié comme un facteur clé de la septicémie, le LPS — alors qualifié d’« endotoxine » — reste aujourd’hui encore au coeur de nombreuses complications infectieuses graves.
Si les chercheurs ont déjà identifié certaines protéines capables de détecter le LPS à l’intérieur des cellules humaines, la manière dont cette reconnaissance s’opère concrètement restait jusqu’ici mal comprise.
Quand la forme de la membrane bactérienne devient un signal d’alerte
« Le problème tient à la structure même du LPS », explique Petr Broz, professeur au Département d’immunobiologie de l’UNIL. « La partie de la molécule responsable de l’activation immunitaire est enfouie dans la membrane bactérienne, ce qui la rend difficilement accessible. »
Pour lever cette énigme, l’équipe lausannoise, en collaboration avec des chercheurs de l’Université de Berne et de République tchèque, s’est intéressée à la géométrie de la membrane bactérienne. Leurs travaux montrent que cette géométrie joue un rôle déterminant dans la détection du LPS.
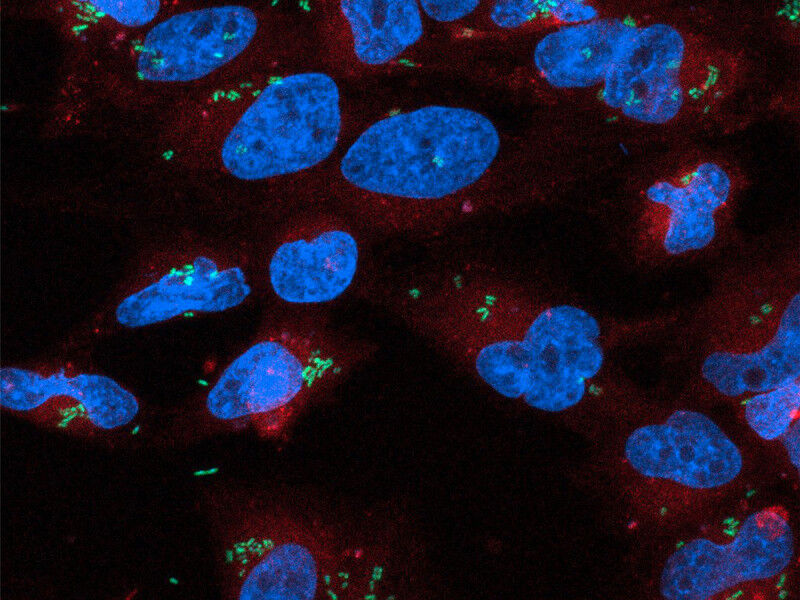
Les bactéries présentes à l’intérieur des cellules sont d’abord ciblées par une enzyme du système immunitaire appelée GBP1. Celle-ci s’assemble à la surface des bactéries et exerce une pression mécanique sur leur membrane, la déformant. Cette contrainte crée des zones de courbure vers l’extérieur, dans lesquelles les molécules de LPS s’écartent légèrement les unes des autres.
« Dans ces régions courbées, les composants lipidiques du LPS deviennent plus exposés », explique Jakub Began, premier auteur de l’étude. Cette exposition permet alors à une autre enzyme, la caspase-4, de se lier au LPS et d’activer une réponse inflammatoire intense, conduisant à la destruction des cellules infectées par un processus appelé pyroptose.
Des implications cliniques majeures
Au-delà de la compréhension fondamentale des mécanismes de l’immunité innée, ces résultats présentent un intérêt clinique considérable. L’activation excessive de la caspase-4 est en effet associée à l’inflammation incontrôlée observée lors du choc septique, une complication potentiellement mortelle.
Les chercheurs ont identifié une poche hydrophobe spécifique de la caspase-4 impliquée dans la liaison au LPS. Cette structure pourrait constituer une cible thérapeutique de choix. « Des molécules capables de bloquer cette interaction pourraient limiter l’inflammation délétère chez les patients atteints d’infections sévères », souligne Petr Broz.
En révélant le rôle clé de la mécanique des membranes bactériennes dans la détection immunitaire, cette étude met en lumière une dimension jusqu’alors largement ignorée des interactions entre l’hôte et les pathogènes. Elle ouvre la voie à de nouvelles stratégies ciblées pour prévenir et traiter les maladies inflammatoires liées aux endotoxines.