Un nouveau gel pourrait lutter contre les bactéries résistantes dans les plaies et autour des implants tout en favorisant la guérison. Des essais sur des animaux avec cet hydrogel inspiré des défenses immunitaires naturelles donnent déjà des résultats prometteurs.
En quelques mots :
- Un hydrogel d’un nouveau genre - c’est-à-dire un gel à base d’eau - ne se contente pas de lutter contre les bactéries, mais apaise les inflammations et favorise ainsi activement la cicatrisation des plaies.
- Le matériau agit comme un filet qui capture les bactéries et les tue sous l’effet d’une impulsion lumineuse.
- Lors d’essais sur des animaux, le gel a montré une forte efficacité contre le germe résistant aux antibiotiques SARM et a accéléré la guérison des plaies.
Les infections bactériennes causent environ 7,7 millions de décès par an dans le monde, et la résistance croissante des bactéries aux antibiotiques ne fait qu’aggraver le problème. Or, les infections dans les plaies sont non seulement de plus en plus difficiles à traiter, mais elles entravent également la guérison des tissus environnants. En effet, elles provoquent une réaction inflammatoire mal dirigée dans laquelle le système immunitaire reste durablement activé, endommage les tissus sains et bloque les processus de réparation nécessaires à la guérison. Les antibiotiques, même s’ils sont efficaces contre les germes, ne peuvent pas faire grand-chose dans ce cas.
Comme les réseaux de protéines de nos cellules immunitaires
C’est précisément là qu’intervient une nouvelle approche que le professeur de l’ETH Raffaele Mezzenga et son équipe, en collaboration avec des chercheurs de l’Université de Shanghai, ont récemment présentée dans la revue spécialisée Nature Communications.
Elle s’inspire des structures protéiques réticulaires que les cellules immunitaires libèrent pour capturer les agents pathogènes et les rendre inoffensifs. Ces pièges extracellulaires à neutrophiles, ou NET, sont une sorte de "filet de capture" naturel qui empêche les infections de se propager dans le corps.
Des tentatives ont déjà été faites pour imiter artificiellement de telles structures. Mais les matériaux synthétiques utilisés se sont parfois révélés trop peu stables, pas assez tolérés ou peu efficaces contre les germes résistants.
Une enzyme antibactérienne activée par la lumière infrarouge
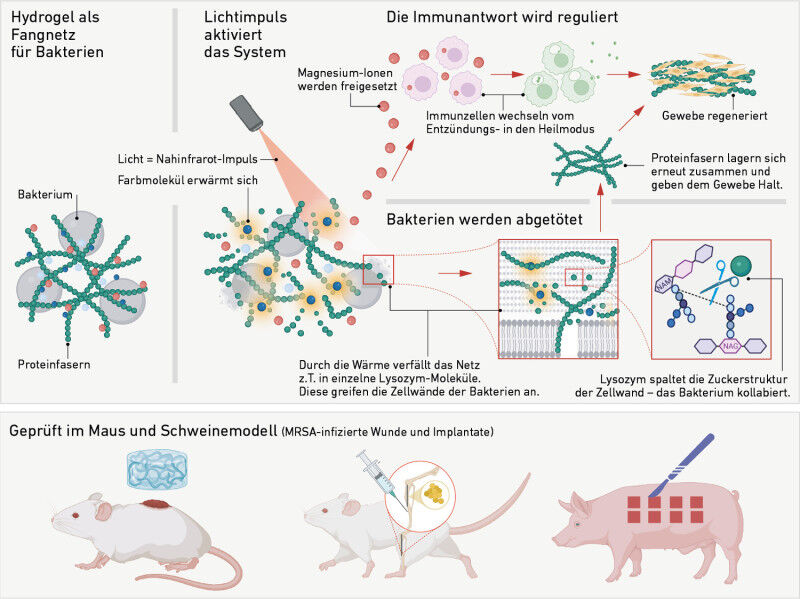
"Contrairement à de nombreuses approches synthétiques, nous misons sur un système naturel à base de protéines", explique Mezzenga. Leur gel est obtenu à partir de blanc d’œuf de poule et se compose d’un réseau dense de minuscules fibres protéiniques de lysozyme encore inactif sous cette forme - une enzyme antibactérienne également présente dans le corps humain. Sous cette forme, le gel agit comme un filet physique qui se pose sur la plaie et retient les bactéries qu’elle contient.
L’étape décisive pour l’activation de l’enzyme n’a lieu qu’en appuyant sur un bouton : lorsque le gel est irradié par une lumière proche de l’infrarouge - une méthode douce et peu invasive - une molécule colorée stockée à cet effet se réchauffe. Sous l’effet de la chaleur générée par la molécule colorée, une partie du réseau de fibres se dissout temporairement et des molécules de lysozyme sont libérées. Dans cet état, elles sont biologiquement actives, comme on l’appelle : elles attaquent de manière ciblée les parois cellulaires des bactéries et les tuent.
Guérison au lieu d’une inflammation permanente
Parallèlement, le gel libère des ions de magnésium lorsqu’il est activé par la lumière. Ceux-ci n’ont pas d’effet antibactérien, mais calment de manière ciblée le système immunitaire : les cellules immunitaires qui favorisent l’inflammation sont reprogrammées en un type de cellules régénératrices. Au lieu d’entretenir les réactions inflammatoires, les cellules soutiennent désormais activement la réparation des tissus - et favorisent ainsi la guérison au lieu de l’entraver.
Dès que l’impulsion lumineuse prend fin, les fibres protéiniques se rassemblent à nouveau en un réseau stable. Le gel se transforme à nouveau en une structure qui soutient les cellules et favorise la régénération des tissus.
La particularité de l’hydrogel réside donc dans la réversibilité des fibres : elles peuvent s’ouvrir et se réunir à nouveau. "Notre technologie combine effet antibactérien, anti-inflammatoire et cicatrisation. Cela pourrait ouvrir de nouvelles possibilités, en particulier pour les patients diabétiques souffrant de plaies chroniques ou de résistances aux antibiotiques", explique Qize Xuan de l’université de Shanghai, premier auteur
Charge bactérienne réduite de 95 pour cent lors d’essais sur animaux
L’hydrogel a déjà été testé dans des études précliniques sur des souris et des porcs. Dans le modèle de souris, le gel a réduit de plus de 95 pour cent la charge bactérienne dans une plaie infectée par le germe MRSA résistant aux antibiotiques. La plaie traitée s’est en outre presque entièrement refermée en 15 jours, tandis que les plaies de contrôle non traitées ont cicatrisé avec un retard considérable. Le modèle porcin a également montré une cicatrisation accélérée de la plaie et une colonisation bactérienne nettement plus faible. De plus, le matériau a créé un environnement favorable à la formation de nouveaux tissus osseux et mous.
Le gel, qui est appliqué directement sur la plaie, reste sur la plaie pendant le processus de guérison. Il pénètre dans les tissus et s’autodétruit progressivement pendant que les tissus se régénèrent.
Mais le chemin est encore long avant que le gel puisse un jour atteindre les patients. La prochaine étape consiste à réaliser des études cliniques. "Nous cherchons maintenant des partenaires industriels pour cela", explique Mezzenga. "De telles études sont complexes, coûteuses et ne sont réalisables qu’en étroite collaboration avec des cliniques."
Référence bibliographique
Xuan Q, Li H, Gao Y, Qiao X, Feng Y, Yu X, Cai J, Jin T, Liu B, Peydayesh M, Su J, Fischer P, Wang P, Chen C, Zhou J, Mezzenga R : NanoNETs amyloïdes photo-réversibles pour des thérapies antimicrobiennes régénératives. Nature Communications, 10 décembre 2025, DOI : https://doi.org/10.1038/s41467-025-65976-6