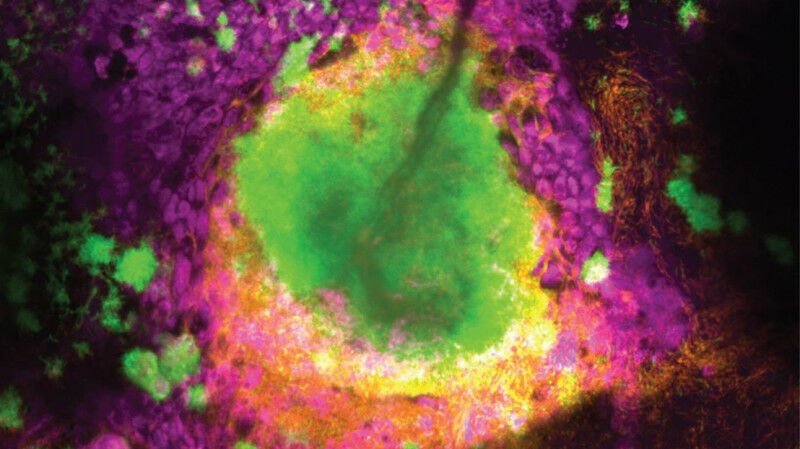
Immaginate di cercare di ambientarvi in una nuova casa mentre siete costantemente sotto attacco. Questo è ciò che deve affrontare il batterio Pseudomonas aeruginosa quando infetta i polmoni. È difficile che si diffonda mentre si protegge dagli antibiotici. Tuttavia, è uno dei principali responsabili delle infezioni nosocomiali ed è noto per provocare infezioni prolungate e resistenti agli antibiotici, causando danni soprattutto nelle persone affette da malattie polmonari come la fibrosi cistica, la BPCO o le bronchiectasie.
Per sopravvivere a condizioni difficili, P. aeruginosa forma colonie note come "biofilm", ossia ammassi di batteri racchiusi in una matrice autoprodotta che conferisce loro notevoli vantaggi, tra cui la protezione dagli antibiotici.
Ma i biofilm hanno un costo: i batteri in ammassi perdono anche la capacità di muoversi, trovare nutrimento e diffondersi in modo efficiente. Per il batterio P. aeruginosa che infetta un polmone, questo pone un dilemma: deve diffondersi sulla superficie del polmone o radicarsi per resistere agli antibiotici? Trovare il giusto equilibrio può significare vita o morte per l’agente patogeno - e alterarlo può significare vita o morte per i pazienti.
Una nuova ricerca condotta dal team di Alexandre Persat dell’Istituto di Infettivologia dell’EPFL ha rivelato come P. aeruginosa gestisca il compromesso tra colonizzazione e sopravvivenza durante l’infezione, passando dalla formazione di un biofilm per proteggere gli antibiotici a uno stato "planctonico" più mobile per diffondersi e accedere ai nutrienti, a seconda delle pressioni ambientali che deve affrontare. Lo studio è stato pubblicato su Nature Microbiology.
Riprodurre ambienti infettivi naturali per osservare i batteri
Per comprendere meglio il comportamento di P. aeruginosa, i ricercatori hanno coltivato i batteri su modelli di tessuto ricoperti di muco che imitano i polmoni umani. Questi modelli di tessuto, noti come "organoidi", sono all’avanguardia nella bioingegneria."Abbiamo quindi utilizzato una tecnica di screening ad alto rendimento chiamata sequenziamento dell’inserzione di trasposoni (Tn-seq), combinata con la modellazione metabolica e l’imaging dal vivo, per studiare come P. aeruginosa si adatta a colonizzare la superficie della mucosa polmonare e a tollerare i trattamenti antibiotici", spiega Lucas Meirelles, che ha guidato lo studio.
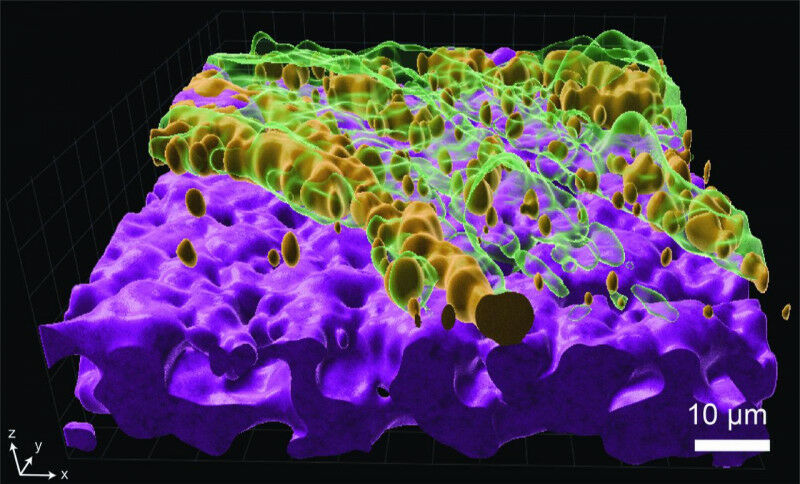
Gli scienziati hanno anche utilizzato la modellazione computerizzata per simulare il modo in cui i batteri metabolizzano i nutrienti nell’ambiente polmonare, contribuendo a determinare le esatte vie metaboliche a cui P. aeruginosa si affida durante l’infezione.
Trovare il giusto equilibrio
Lo studio ha rivelato che la P. aeruginosa si adatta al muco polmonare facendo affidamento su zuccheri e lattato, nutrienti abbondanti nei polmoni infetti. Tuttavia, per sopravvivere nel muco, il batterio deve anche sintetizzare nutrienti essenziali meno disponibili, come gli aminoacidi. Questa autosufficienza, o "indipendenza metabolica", aiuta i batteri a prosperare nelle prime fasi dell’infezione polmonare.Il team di Alexandre Persat ha scoperto il meccanismo alla base di questo dilemma. Si è reso conto che la formazione del biofilm impone un "onere metabolico". In altre parole, la produzione della matrice appiccicosa che tiene insieme il biofilm consuma risorse, rallentando la capacità di diffusione dei batteri. Negli esperimenti, i batteri che non riuscivano a formare biofilm si diffondevano in modo più efficiente, ma rimanevano vulnerabili agli antibiotici. Questa nuova visione dei costi metabolici della formazione del biofilm spiega come i batteri riescano a conciliare crescita e tolleranza agli antibiotici.
Lo studio evidenzia il delicato gioco di equilibri che lo Pseudomonas aeruginosa deve compiere durante le infezioni. Sebbene i batteri debbano colonizzare i polmoni in modo efficiente, la loro migliore strategia di sopravvivenza - la formazione di biofilm - limita il loro accesso ai nutrienti e quindi la loro capacità di diffondersi. Tuttavia, una volta introdotti gli antibiotici, la formazione del biofilm diventa vantaggiosa, impedendo ai batteri di essere eliminati.
Esplorare nuove strade
Questa scoperta apre la strada all’esplorazione di nuove strategie terapeutiche: se riusciamo a interrompere la capacità dei batteri di formare biofilm senza dare loro più spazio per diffondersi, potremmo renderli più vulnerabili ai trattamenti esistenti. Inoltre, i trattamenti che mirano alle vie metaboliche dei batteri potrebbero rivelarsi efficaci per alleviare le infezioni da Pseudomonas.Più in generale, gli scienziati ritengono che lo studio di agenti patogeni come la P. aeruginosa in modelli di infezione che riproducono la fisiologia dei tessuti umani sia essenziale nella lotta alla resistenza agli antibiotici.
La resistenza agli antibiotici è destinata a diventare una delle più gravi sfide sanitarie di questo secolo e P. aeruginosa è uno dei principali protagonisti di questo problema", afferma Lucas Meirelles. Utilizzando l’ingegneria tissutale per riprodurre l’ambiente delle vie aeree in laboratorio, stiamo cercando di comprendere meglio la fisiologia di questo patogeno. In questo modo, speriamo di scoprire bersagli precedentemente sconosciuti che ci aiutino a combattere queste infezioni e a contrastare la resistenza agli antibiotici".