Una volta che uno spermatozoo ha raggiunto una cellula uovo per fecondarla, i due devono rimanere uniti in modo molto stretto. Questo avviene grazie a un legame proteico che è uno dei più forti della biologia e che è anche unico nel suo genere.
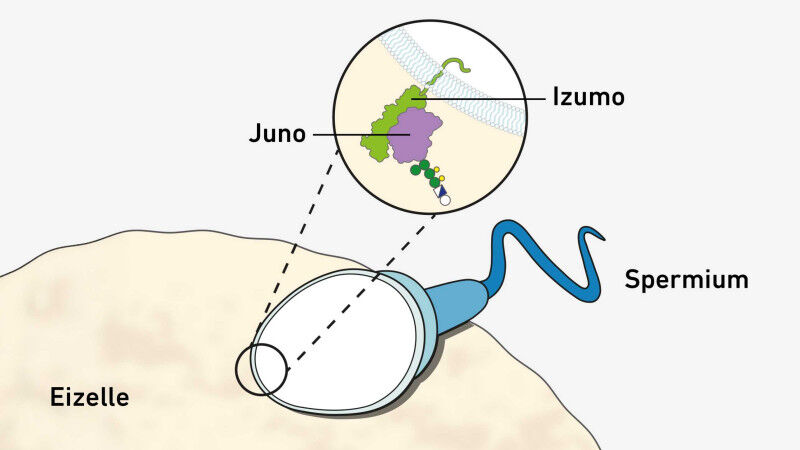
Una cellula uovo e una cellula spermatica devono aderire saldamente l’una all’altra nella tuba di Falloppio per potersi fondere e, di conseguenza, creare un nuovo essere vivente. La proteina Juno sulla membrana cellulare dell’uovo e la proteina Izumo sullo spermatozoo svolgono un ruolo centrale in questo processo. I ricercatori del Politecnico di Zurigo e dell’Università di Basilea sono ora riusciti a dimostrare che le due proteine sono collegate: Il legame tra le due proteine è speciale e uno dei più forti finora conosciuti nel mondo degli organismi multicellulari.
Per raggiungere la membrana cellulare della cellula uovo, lo spermatozoo deve lavorare sodo. Spinto dal suo flagello, la proiezione rotante a forma di frusta, deve prima farsi strada attraverso due strati protettivi che circondano la cellula uovo.
Una volta che lo spermatozoo è riuscito a raggiungere la membrana cellulare della cellula uovo, deve resistere e guadagnare tempo. Questo è necessario perché le membrane dell’ovulo e dello spermatozoo devono essere riorganizzate in modo da diventare più flessibili e potersi fondere. Inoltre, le proteine di membrana importanti per la fusione devono essere riunite nel punto giusto. Per esempio, il flagello nella parte posteriore dello spermatozoo si agita selvaggiamente, mentre nella parte anteriore la coppia di proteine Juno-Izumo, con il suo forte legame, assicura che lo spermatozoo non si stacchi di nuovo dall’uovo.
Aggancio delle dita su scala nanometrica
I ricercatori di Zurigo e Basilea hanno analizzato più da vicino le due proteine Juno e Izumo. Lo hanno fatto indipendentemente dalla cellula uovo e dallo spermatozoo: in laboratorio hanno fissato una proteina Juno e una Izumo in un microscopio a forza atomica e hanno misurato la capacità delle due proteine di tenersi reciprocamente quando vengono tirate. Il principio di misurazione è simile a quello di due persone che uniscono le loro dita medie e poi tirano fino a quando la connessione si rompe.
In questo modo, gli scienziati hanno dimostrato che Juno e Izumo si comportano diversamente dalla maggior parte delle coppie di proteine conosciute, che formano un legame secondo il principio del lock-and-key. Tali legami proteici non durano per sempre. E per la maggior parte di essi, quanto più forte è la trazione, tanto più breve è la durata.
Juno e Izumo sono diversi. "In presenza di forze di trazione, come quelle generate dagli spermatozoi, il legame non diventa meno stabile, ma più stabile", spiega Viola Vogel, docente presso il Dipartimento di Scienze e Tecnologie della Salute del Politecnico di Zurigo. "In questo modo, il legame dura ancora più a lungo sotto la forza di trazione rispetto a quando non viene applicata la forza" In questo caso, i ricercatori parlano di legame di cattura - un legame rinforzato dalla forza di trazione.
Vogel e i suoi colleghi hanno condotto il loro studio insieme al gruppo di Michael Nash, professore presso il Dipartimento di Scienza e Ingegneria dei Biosistemi del Politecnico di Zurigo e dell’Università di Basilea.
Una delle connessioni più forti
Utilizzando i modelli di calcolo del Centro Nazionale Svizzero di Supercalcolo CSCS di Lugano, i ricercatori sono stati in grado di mostrare come funziona il meccanismo di catch-bond delle due proteine: Quando le proteine vengono allontanate, alcuni legami tra gli atomi di una proteina si rompono con gli atomi dell’altra proteina. Allo stesso tempo, però, le due proteine ruotano l’una rispetto all’altra mentre vengono allontanate - la proteina Juno compie un quarto di giro. Questo crea nuovi legami atomo-atomo. Questi legami prolungano il tempo in cui le due proteine rimangono collegate tra loro.
Le misurazioni effettuate dai ricercatori hanno dimostrato che, sotto tensione, il legame tra Juno e Izumo è uno dei più forti nel regno degli organismi multicellulari. Anche nelle fibre muscolari esistono legami altrettanto forti tra le proteine, che impediscono alle fibre muscolari di strapparsi. Anche altre cellule che devono aderire alle superfici del corpo lo fanno con proteine che formano legami di cattura. Ad esempio, le cellule immunitarie che aderiscono all’interno dei vasi sanguigni o le cellule cutanee di nuova formazione che aderiscono alle fibre dell’ambiente durante la guarigione delle ferite.
La mutazione nota indebolisce il legame proteico
Infine, i ricercatori hanno studiato anche le conseguenze di una mutazione genetica nota che colpisce una donna su 600 in tutto il mondo. In queste donne, sia il gene Juno che la proteina Juno sono alterati in un componente. Si sospetta che la mutazione riduca la fertilità.
Gli scienziati hanno anche analizzato le proteine alterate corrispondenti in laboratorio e con simulazioni al computer e sono riusciti a dimostrare che la mutazione può ridurre la fertilità: Quando è sottoposta a forze di trazione, come quelle che si verificano durante il battito flagellare degli spermatozoi, una connessione con una proteina alterata si rompe più rapidamente. "Questo non dà allo spermatozoo e alla cellula uovo il tempo sufficiente per fondersi e quindi avviare la fecondazione", spiega Vogel.
Poiché il legame precedentemente sospettato tra questa mutazione e l’infertilità è stato ora confermato attraverso un meccanismo, il prossimo passo potrebbe essere lo sviluppo di test genetici appropriati per diagnosticare questa causa di infertilità. Inoltre, i risultati potrebbero favorire lo sviluppo di terapie per aiutare le coppie a realizzare il loro desiderio di avere figli.
Riferimento alla letteratura
Boult S, Pacak P, Yang B, Liu H, Vogel V, Nash MA: Riorganizzazione dipendente dalla forza e meccanostabilità del complesso Izumo1:Juno coinvolto nella fecondazione umana. Nature Communications 2025, doi: 10.1038/s41467-025-62427-0