Il cancro è innegabilmente complesso e ogni tumore risponde a terapie diverse. Questo vale anche per i linfomi, un tipo di cancro del sangue che ha origine nei linfociti, un sottogruppo di cellule immunitarie che aiutano a combattere le infezioni. Gli scienziati cercano costantemente di individuare la terapia migliore per ogni paziente.
I metodi tradizionali per testare l’efficacia delle terapie contro i linfomi sono limitati. Ad esempio, i modelli di xenotrapianto derivati da pazienti, in cui tumori umani vengono coltivati su topi, sono efficaci ma anche lenti e costosi. Inoltre, non colgono appieno la diversità delle interazioni tra il tumore e le cellule immunitarie.
Più recentemente, gli scienziati hanno iniziato a sviluppare "avatar tumorali", nuovi sistemi per conservare cellule o campioni di tessuto al di fuori del corpo del paziente(ex vivo). Gli avatar tumorali sono strumenti molto promettenti. Tuttavia, è stato particolarmente difficile preservare la struttura e la composizione cellulare originale dei linfomi.
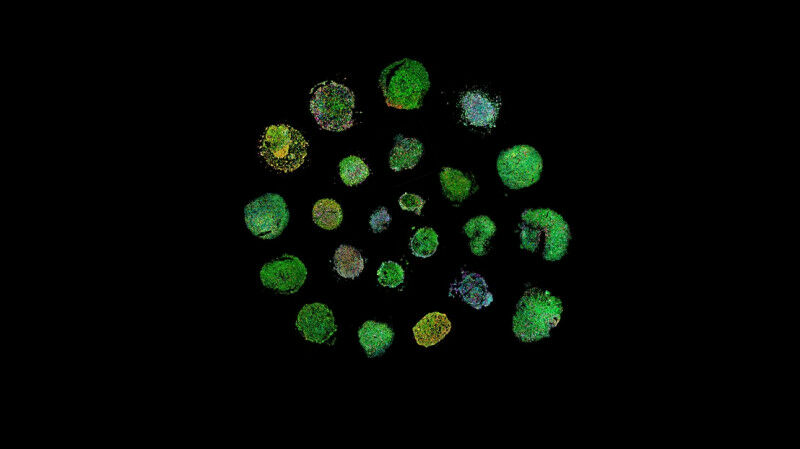
Per affrontare queste sfide, Albert Santamaria-Martínez ed Elisa Oricchio dell’EPFL, in stretta collaborazione con i medici del CHUV, hanno sviluppato un modello avanzato ex vivo chiamato "linfomoidi". Hanno identificato un ambiente specifico che consente di mantenere in vita frammenti di tessuto di linfoma per diversi giorni. In queste condizioni, sono riusciti a preservare l’architettura, la diversità cellulare e il microambiente del tumore.
I ricercatori hanno raccolto 27 campioni di linfoma umano e hanno dimostrato, utilizzando analisi basate sull’imaging e profili molecolari spaziali, che i linfoidi mantengono le caratteristiche fenotipiche e molecolari dei tumori originali.
In uno studio su diversi tipi di linfoma umano a cellule B, i linfoidi sono stati mantenuti vivi e strutturalmente intatti per diversi giorni, consentendo ai ricercatori di esaminare la risposta dei campioni a diversi farmaci. L’équipe ha testato sui linfoidi una serie di farmaci antitumorali, tra cui gli inibitori della tirosin-chinasi di Bruton (BTK), gli inibitori della PI3K e gli inibitori della BCL-2, per determinare se questi trattamenti potessero ridurre la crescita e la proliferazione delle cellule di linfoma.
I linfomi hanno mostrato una gamma di sensibilità ai farmaci antitumorali, rispecchiando fedelmente le risposte cliniche dei pazienti di cui sono stati utilizzati i campioni di tessuto. Ad esempio, i linfomi di un paziente il cui tumore ha risposto bene agli inibitori di BTK hanno mostrato sensibilità allo stesso farmaco nel modello ex vivo. In un altro caso, i linfomi di un paziente resistente alla lenalidomide hanno mostrato una resistenza simile nei test ex vivo.
Questa ricerca suggerisce che i linfoidi possono servire come strumento affidabile per prevedere come i singoli pazienti possono rispondere a trattamenti specifici. Consentendo ai ricercatori di testare l’efficacia dei farmaci su campioni derivati dai pazienti, i linfoidi offrono un nuovo promettente modo di personalizzare il trattamento del cancro. Potrebbero consentire ai medici di utilizzare il campione di tessuto di un paziente per trovare il trattamento più efficace per quella persona prima di iniziare la terapia, risparmiando ai pazienti trattamenti inutili ed effetti collaterali.
I linfoidi potrebbero anche essere utilizzati negli studi clinici per testare nuove terapie antitumorali ed esplorare le complesse dinamiche tra cellule tumorali e cellule immunitarie durante il trattamento.
Salute personalizzata e tecnologie correlate (PHRT)
Fondazione ISREC
Fondazione Aclon
Fondazione Accentus
Fondazione San Salvatore