I ricercatori hanno sviluppato un microrobot in grado di trasportare farmaci in aree specifiche del corpo e che potrebbe essere presto utilizzato negli ospedali.
Ogni anno, in tutto il mondo, dodici milioni di persone vengono colpite da ictus, molte delle quali muoiono o rimangono invalide. Per sciogliere il trombo che blocca il vaso sanguigno, oggi si somministrano farmaci che vengono distribuiti in tutto il corpo. Per garantire che la quantità di farmaco necessaria raggiunga il trombo, è necessario somministrare una dose elevata. Questo può portare a effetti collaterali significativi, come emorragie interne. Poiché i farmaci sono spesso necessari solo in un punto specifico del corpo, la ricerca medica sta cercando da tempo di distribuire i farmaci nel punto in cui devono agire: Nel caso di un ictus, direttamente in prossimità del trombo. Ora un gruppo di ricercatori ha raggiunto una svolta decisiva a diversi livelli, che ha pubblicato sulla rivista Science.
Sono necessarie nanoparticelle di precisione
I ricercatori utilizzano come microrobot una capsula rotonda da loro sviluppata, costituita da un involucro di gel dissolvibile, che possono guidare magneticamente attraverso il corpo e quindi portare a destinazione. Le nanoparticelle di ossido di ferro contenute nella capsula forniscono le proprietà magnetiche. "Poiché i vasi del cervello umano sono così piccoli, la capsula può avere solo una certa dimensione. La sfida tecnica consiste nel garantire che una capsula così piccola abbia anche proprietà magnetiche sufficientemente forti", spiega Fabian Landers, primo autore dell’articolo e ricercatore post-dottorato presso il Multi-Scale Robotics Lab del Politecnico di Zurigo.
È inoltre necessario un agente di contrasto che consenta ai medici di utilizzare le immagini a raggi X per vedere come la capsula si muove nei vasi. I ricercatori hanno utilizzato nanoparticelle di tantalio, spesso usate in medicina, ma più difficili da controllare perché più pesanti. "Combinare funzionalità magnetica, visibilità delle immagini e controllo preciso in un unico microrobot richiede un’interazione perfetta tra scienza dei materiali e robotica. Ci sono voluti molti anni per raggiungere questo obiettivo", afferma il professor Bradley Nelson dell’ETH, che da decenni si occupa di ricerca sui microrobot. Il professor Salvador Pané, chimico presso l’Istituto di Robotica e Sistemi Intelligenti, e il suo team hanno sviluppato nanoparticelle di ossido di ferro perfettamente adattate che rendono possibile questo sofisticato equilibrio.
Un catetere speciale rilascia la capsula con il farmaco
I microrobot contengono anche il principio attivo che devono trasportare. I ricercatori sono riusciti a caricare i microrobot con farmaci comuni per varie applicazioni. Tra questi, un farmaco che scioglie i trombi, un antibiotico e un farmaco antitumorale. I farmaci vengono rilasciati da un campo magnetico ad alta frequenza, che riscalda le nanoparticelle magnetiche e quindi scioglie il guscio di gel e il microrobot.
Per avvicinare il microrobot al bersaglio, i ricercatori utilizzano innanzitutto un catetere di inserimento. Il catetere ha un filo guida interno collegato a una pinza flessibile in polimero. Quando questo viene spinto oltre la guida esterna, la pinza polimerica si apre e rilascia il microrobot. I ricercatori hanno quindi guidato il microrobot magnetico nella posizione corretta utilizzando un sistema di navigazione magnetica.
Controcorrente: la navigazione nei vasi sanguigni
Per controllare con precisione i microrobot, i ricercatori hanno sviluppato un sistema di navigazione elettromagnetico modulare, adatto all’uso in sala operatoria. "La velocità del sangue nel sistema arterioso umano varia notevolmente a seconda della posizione. Questo rende la navigazione di un microrobot molto complessa", spiega Nelson. I ricercatori hanno combinato tre diverse strategie di navigazione magnetica tra loro, consentendo loro di navigare in tutte le regioni delle arterie della testa.
Ad esempio, possono far rotolare la capsula lungo la parete del vaso utilizzando un campo magnetico rotante. La capsula può essere guidata con estrema precisione verso il bersaglio a una velocità di 4 millimetri al secondo.
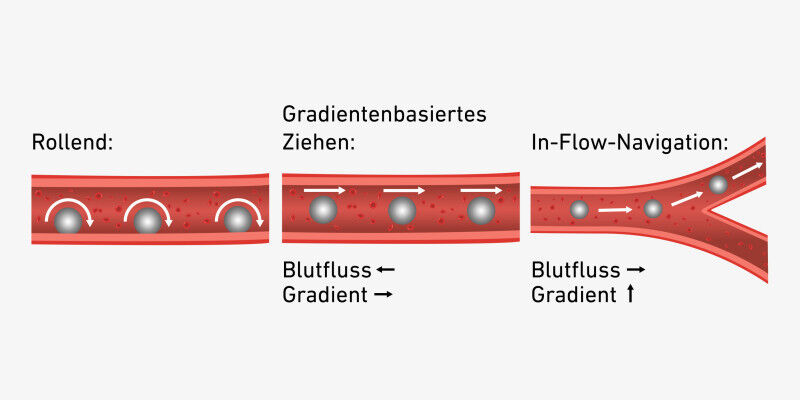
In un’altra variante, la capsula viene spostata con un gradiente di campo magnetico: il campo magnetico è più forte in un punto rispetto a un altro. Il microrobot viene così trascinato all’interno della nave nella direzione del campo più forte. La capsula può anche nuotare controcorrente, a una velocità di flusso notevole, superiore a 20 centimetri al secondo "È incredibile quanto sangue venga pompato attraverso i nostri vasi e a quale velocità. Il nostro sistema di navigazione deve essere in grado di resistere a tutto questo", spiega Landers.
Quando il microrobot raggiunge un ramo dei vasi attraverso il quale sarebbe difficile manovrare, entra in gioco la navigazione in flusso. Il campo magnetico viene applicato alla parete del vaso in modo tale che la capsula venga trascinata nel vaso corretto.
Combinando le tre varianti di navigazione, i ricercatori sono in grado di controllare i microrobot in modo robusto in diverse condizioni di flusso e scenari anatomici. La capsula ha consegnato con successo il farmaco nella posizione corretta in oltre il 95% dei casi testati. "I campi magnetici sono ideali per le procedure minimamente invasive perché penetrano in profondità nel corpo e, alle intensità e frequenze da noi utilizzate, non hanno alcun effetto sul corpo", spiega Nelson.
L’innovazione non si è fermata al robot
Per testare i microrobot e la loro navigazione in un ambiente realistico, i ricercatori hanno sviluppato modelli in silicone in cui hanno modellato con precisione i vasi di pazienti e animali. Questi modelli vascolari sono così realistici che ora vengono utilizzati per la formazione dei medici e sono distribuiti dallo spin-off Swiss Vascular dell’ETH. "I modelli sono molto importanti per noi perché abbiamo dovuto esercitarci molto spesso per ottimizzare la strategia e tutti i componenti. Non è possibile farlo negli animali", spiega Pané. Nel modello, i ricercatori sono riusciti a sciogliere un coagulo di sangue in modo mirato.
Dopo molti esperimenti di successo nel modello, il team ha voluto dimostrare cosa il microrobot potesse fare in condizioni cliniche reali. In primo luogo, sono riusciti a dimostrare nei maiali che tutti e tre i metodi di navigazione funzionano e che il microrobot rimane chiaramente visibile durante la procedura. In secondo luogo, hanno fatto navigare i microrobot nel liquido cerebrospinale di una pecora. Landers è particolarmente soddisfatto: "Questo complesso ambiente anatomico ha un grande potenziale per ulteriori interventi terapeutici, ed è per questo che è stato così eccitante per noi che il microrobot abbia trovato la sua strada anche qui"
Non solo per le occlusioni vascolari
I nuovi microrobot potrebbero essere utilizzati non solo per le trombosi, ma anche per le infezioni o i tumori localizzati. In ogni fase dello sviluppo, il team di ricerca ha tenuto conto del fatto che tutto ciò che è stato messo a punto potrà essere utilizzato al più presto anche in sala operatoria. Il prossimo obiettivo è quello di avviare al più presto gli studi clinici sull’uomo. Fabian Landers parla della motivazione che guida l’intero team: "I medici stanno già facendo un lavoro incredibile in ospedale. Il fatto di avere tra le mani una tecnologia che ci permette di aiutare i pazienti in modo più rapido ed efficace e di dare loro nuove speranze attraverso terapie innovative è ciò che ci spinge."
Riferimento alla letteratura
Landers F, Hertle L, Pustovalov V et al: Microrobot magnetici clinicamente pronti per terapie mirate. Scienza 2025, adx1708