Gli scienziati dell’EPFL e della Johns Hopkins University hanno rivelato il ruolo centrale di un enzima nel controllo dei sottotipi di cancro alla prostata e nel miglioramento della risposta terapeutica.
Un team guidato da Wouter Karthaus, capo del Laboratorio di resistenza alle terapie endocrine e genetica molecolare dell’EPFL, e da Eneda Toska della Johns Hopkins University ha identificato l’enzima KMT2D come regolatore epigenetico chiave del cancro alla prostata. Il loro studio rivela che KMT2D svolge un ruolo centrale nel modo in cui i tumori della prostata si sviluppano, sopravvivono e rispondono ai trattamenti.
Cancro alla prostata resistente
La maggior parte dei tumori della prostata dipende dal recettore degli androgeni per alimentare la propria crescita. Questi tumori vengono generalmente trattati con terapie ormonali che bloccano la segnalazione del recettore degli androgeni.
Tuttavia, con il tempo, molti tumori della prostata si adattano e diventano resistenti, dando origine al "cancro della prostata resistente alla castrazione" (CRPC). Alcuni CRPC rimangono dipendenti dal recettore degli androgeni, ma altri si liberano completamente, diventando più difficili da trattare.
Un enzima chiave
È qui che entra in gioco KMT2D. I ricercatori hanno scoperto che questo enzima facilita l’accesso del recettore degli androgeni ai geni chiave coinvolti nella crescita del tumore e nella loro attivazione. Lo fa modificando la struttura della cromatina, che è il denso involucro proteico del DNA nella cellula.
In questo modo, il recettore degli androgeni e le sue proteine ausiliarie possono accedere ai loro siti bersaglio in modo più efficiente. Ciò contribuisce a mantenere l’attività dei tumori della prostata dipendenti dal recettore degli androgeni, che hanno bisogno di questa via per continuare a svilupparsi.
Lo studio ha anche rivelato che KMT2D svolge un ruolo essenziale in una forma particolarmente aggressiva di cancro alla prostata indipendente dal recettore degli androgeni, nota come sottotipo "simile alle cellule staminali". In questi tumori, KMT2D mantiene un’identità cellulare ibrida regolando una serie diversa di fattori di trascrizione, tra cui quelli della famiglia AP-1, come FOSL1, che sono collegati al comportamento simile alle cellule staminali e alla resistenza al trattamento.
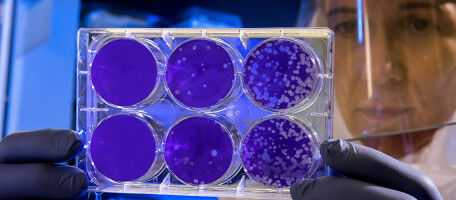
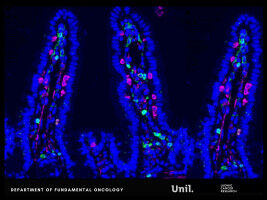
Gli scienziati hanno fatto questa scoperta utilizzando linee cellulari di cancro alla prostata geneticamente modificate, organoidi derivati da pazienti, sequenziamento di singole cellule e modelli animali. La delezione o l’inibizione di KMT2D ha interrotto la capacità delle cellule tumorali di mantenere la propria identità e le ha rese più vulnerabili al trattamento.
In modelli preclinici, il blocco di KMT2D ha amplificato l’efficacia di alcuni farmaci antitumorali (inibitori di PI3K/AKT e inibitori del recettore dell’adenosina).
Conseguenze
I risultati suggeriscono che KMT2D potrebbe essere un interessante bersaglio terapeutico nel cancro alla prostata. La sua disattivazione potrebbe rendere i tumori responsivi ai trattamenti esistenti o rallentare la loro progressione verso forme più aggressive. Il lavoro evidenzia anche l’importanza di adattare i trattamenti a specifici sottotipi di tumore e di utilizzare il profilo epigenetico per guidare le decisioni terapeutiche.
Secondo Wouter Karthaus, "Con il continuo aumento dei casi di cancro alla prostata e il conseguente incremento del numero di pazienti che sviluppano una malattia resistente ai farmaci, è importante capire come il cancro alla prostata diventa resistente ai farmaci e scoprire nuove strade terapeutiche. KMT2D rappresenta questa nuova via"
Riferimenti
Srushti Kittane, Erik Ladewig, Taibo Li, Jillian R. Love, Ryan Blawski, Yangzhenyu Gao, Amaia Arruabarrena-Aristorena, Peihua Zhao, Susan Dalrymple, Huayang Liu, Xinyu Guo, Mirna Sallaku, Nachiket Kelkar, Liliana Garcia Martinez, Javier Carmona Sanz, Wanlu Chen, Candice Stoudmann, Laura Baldino, Milad Razavi-Mohseni, Ingrid Kalemi, Michael A. Beer, Pau Castel, W. Nathaniel Brennen, Maurizio Scaltriti, Lluis Morey, Emiliano Cocco, Hongkai Ji, Ho Man Chan, Alexis Battle, Christina Leslie, Wouter R. Karthaus, Eneda Toska. L’istone metiltransferasi KMT2D è un mediatore critico della plasticità del lignaggio e della risposta terapeutica nel cancro alla prostata resistente alla castrazione. Cancer Research 11 dicembre 2025. DOI: 10.1158/0008-5472.CAN-25-2053