Wissenschaftler der Universität Genf haben einen neuen Mechanismus entdeckt, der an der Regulierung des Blutdrucks beteiligt ist, und damit den Weg für neue therapeutische Ansätze geebnet.
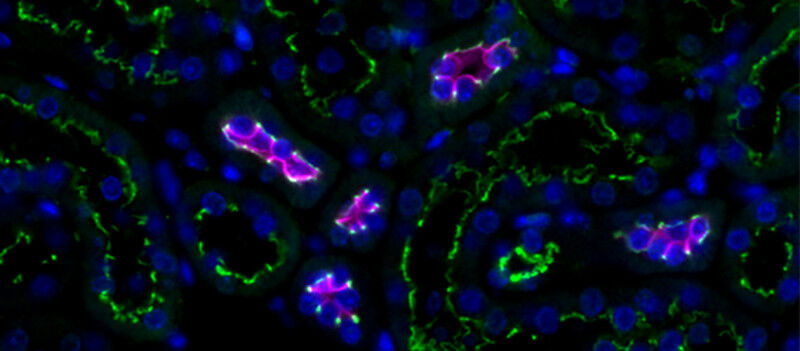
Bluthochdruck betrifft fast jeden dritten Erwachsenen auf der Welt und ist einer der Hauptrisikofaktoren für Herz-Kreislauf-Erkrankungen. Frühere Studien legen nahe, dass ein Protein, das Paracingulin, bei seiner Entstehung eine Rolle spielt, doch die zugrunde liegenden Mechanismen sind noch nicht ausreichend verstanden. Wissenschaftler der Universität Genf haben ein Mausmodell entwickelt, um zu verstehen, warum der Verlust von Paracingulin die Entwicklung von Bluthochdruck abschwächt. Das Team bestätigt nun seine entscheidende Rolle bei der Entstehung von Bluthochdruck und liefert eine gründliche Analyse dieses Mechanismus. Die Ergebnisse sind in der Fachzeitschrift American Journal of Physiology, Renal Physiology zu lesen.
Der Blutdruck ist die Kraft, die das Blut ausübt, wenn es durch die Blutgefässe fliesst. Er wird von mehreren Faktoren reguliert, unter anderem von den Nieren. Sie filtern das Blut und kontrollieren die Menge an Salz und Wasser, die mit dem Urin ausgeschieden wird, was sich direkt auf das Blutvolumen und damit auf den Druck auswirkt. Hinzu kommen Hormone wie Angiotensin II oder Aldosteron, die den Körper dazu bringen, Natrium zurückzuhalten und die Gefässe zu verengen. Dieses Regulationssystem sorgt dafür, dass der Blutdruck in einem optimalen Bereich bleibt, aber es kann aus dem Gleichgewicht geraten und zu Bluthochdruck führen, einem Hauptrisikofaktor für die Herz-Kreislauf-Gesundheit.
Unsere Ergebnisse legen nahe, dass der Schutz vor Bluthochdruck mit der Funktion der Nieren zusammenhängt und nicht mit der Kontraktion der Blutgefässe.
Die Dahl-Ratte zur Untersuchung von Bluthochdruck
Es gibt ein Tiermodell, die Dahl-Ratte (benannt nach dem amerikanischen Forscher, der dieses Modell entwickelt hat), das seit mehreren Jahrzehnten zur Untersuchung von Bluthochdruck verwendet wird. Diese Rattenlinie entwickelt spontan einen hohen Blutdruck, wenn die Tiere mit einer salzreichen Diät gefüttert werden. Es wurde jedoch beobachtet, dass diese Ratten, die einer salzhaltigen Diät ausgesetzt wurden, in Abwesenheit des Zellverbindungsproteins Paracingulin (CGNL1) keinen Bluthochdruck entwickelten.
Sandra Citi, assoziierte Professorin an der Abteilung für Molekular- und Zellbiologie der naturwissenschaftlichen Fakultät der Universität Genf, ist Spezialistin für interzelluläre Verbindungen. Diese Proteinriegel verbinden benachbarte Zellen miteinander, um die Integrität des Gewebes zu gewährleisten und den Durchgang von Ionen oder Nährstoffen durch die Zellkompartimente zu kontrollieren. In Zusammenarbeit u.a. mit Eric Feraille, ordentlicher Professor an der Abteilung für Zellphysiologie und Stoffwechsel der Medizinischen Fakultät der Universität Genf und Spezialist für Nierenphysiologie, untersuchte das Team von Sandra Citi die Rolle von Paracingulin bei Bluthochdruck. Nachdem sie die Genmutation CGNL1 in Mäusen erzeugt hatten, beobachteten sie, dass der Verlust von Paracingulin vor Bluthochdruck schützt, der durch die Infusion von Angiotensin II induziert wird.
Eine spezifische Wirkung auf die Nieren
Angiotensin-II-induzierter Bluthochdruck führt normalerweise zu einer Aktivierung der Natrium-(Salz-)Transporter in der Niere. Die Wissenschaftler analysierten daher die Werte der aktivierten Transporter in der Niere in Abwesenheit von Paracingulin. ’Wir konnten keine Aktivierung der Transporter beobachten. Unsere Ergebnisse legen daher nahe, dass der Schutz vor Bluthochdruck mit der Funktion der Niere zusammenhängt und nicht mit der Kontraktion der Blutgefässe’, erklärt Florian Rouaud, Oberassistent am Departement für Molekular- und Zellbiologie der naturwissenschaftlichen Fakultät der Universität Genf und Erstautor der Studie. ’Wenn CGNL1 fehlt, kann Angiotensin II bestimmte Natriumtransporter in den Nierentubuli nicht mehr aktivieren, was den Körper daran hindert, Wasser und Salz zurückzuhalten, und somit den Druck erhöht.
Ein neuartiger therapeutischer Ansatz
Diese Studie identifiziert Paracingulin zum ersten Mal als einen Schlüsselakteur in der renalen Angiotensin-II-Signalgebung, einem Weg, von dem bisher nicht bekannt war, dass Junktionalproteine daran beteiligt sind. Sie könnte letztendlich die Entwicklung neuer therapeutischer Strategien ermöglichen, die auf dieses Protein abzielen und die derzeitigen Behandlungen ergänzen, die häufig auf Inhibitoren des Renin-Angiotensin-Systems basieren.
Die Forschungsergebnisse werden in
American Journal of Physiology, Renal Physiology veröffentlicht
DOI: 10.1152/ajprenal.00271.2024